Jon glinu i fluorek wykazują zdolność tworzenia stabilnych kompleksów (Al-F). Stale podejmowane są próby badań interakcji między tymi jonami oraz związku powstałych kompleksów z fluorozą. Dowiedziono np., że glin – zaburzając absorpcję fluorku – wpływa na redukcję fluorozy u zwierząt, natomiast stosunkowo nieduże dawki wodorotlenku glinu u ludzi mogą istotnie zmniejszać ilość pobieranego fluorku, a zwiększać wydalanie.
Zainteresowanie badaczy kompleksami Al-F i ich związkami z zaburzeniami mineralizacji i fluorozą nieustannie rośnie.
Ciemne i jasne strony fluorków
Fluorki (F-) są absorbowane do naszego ustroju przede wszystkim przez przewód pokarmowy i płuca. Wchłanianie jest szybsze w środowisku o niskim pH. Spożywanie produktów zawierających m.in. związki glinu ogranicza absorpcję fluorków w przewodzie pokarmowym przez tworzenie trudno rozpuszczalnych soli. Jon fluorkowy z osocza krwi przenika do tkanek (kumuluje się w kościach) lub do nerek (jest wydalany).
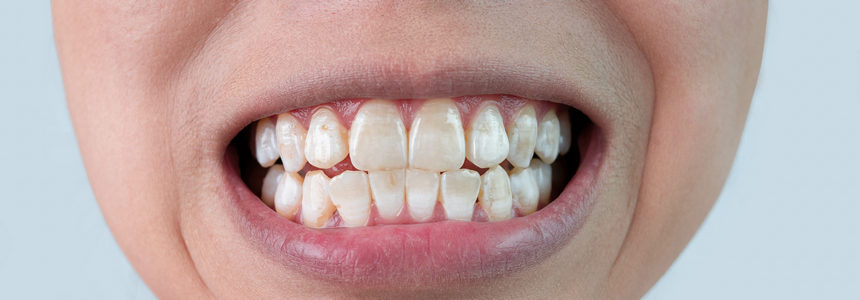
Dzięki badaniom nad oddziaływaniem związków fluoru na nasze zdrowie udało się ustalić znamienną zależność między fluorkami a próchnicą zębów. Wykazano, że skuteczna profilaktyka próchnicy polega na miejscowym działaniu fluorków na szkliwo. Fluorki zaburzają proces demineralizacji, przyspieszają remineralizację i hamują procesy wytwarzania kwasów przez płytkę bakteryjną. Jednak nadmierna ekspozycja na fluorki (długotrwała, zbyt duże dawki) może wywierać niekorzystny wpływ na zdrowie człowieka (m.in. osłabiać układ immunologiczny i układ nerwowy, prowadzić do ospałości lub depresji). Skutkiem zbyt dużych dawek fluorków jest fluoroza – choroba ogólnoustrojowa powodująca uszkodzenie wątroby, nerek, zaburzenia wzroku. Jedną z jej charakterystycznych manifestacji jest cętkowane zabarwienie na zębach i wzrost ich kruchości. To konsekwencja uszkodzenia ameloblastów (komórek budujących szkliwo) przez nadmiar tego pierwiastka, a także jego hamującego wpływu na działanie enzymów, co utrudnia mineralizację szkliwa. Podejrzewa się, że w rozwoju fluorozy szkliwa biorą udział białka G ameloblastów (białka te mogą uczestniczyć w zaburzeniach drogi sekrecyjnej ameloblastów we fluorozie szkliwa). Skutkiem mogą być także niekorzystne zmiany w układzie kostnym. W wyniku pogrubienia w kościach warstwy koronowej dochodzi do skrzywień i deformacji kręgosłupa. Odkładanie związków fluoru w kościach różni się zależnie od wieku – największą kumulację potwierdzono u dzieci (ponad 50%) i młodzieży (50%), znacznie niższa jest u seniorów (ok. 10%).
Jednorazowe przyjęcie zbyt dużej ilości fluoru powoduje objawy typowe dla zatruć ostrych, jak: biegunka, ból brzucha, hipokalcemia, drgawki, wymioty. Szczególnie niebezpieczny jest nadmiar związków fluoru spożywany przez kobiety w ciąży. Wzrost stężenia fluoru w surowicy krwi matki skutkuje dyfuzją przez barierę łożyskową i jest szkodliwy dla rozwoju płodu, może np. wpływać na zmniejszenie masy noworodka (i jego szanse przeżycia).
Tymczasem – jeśli glin może antagonizować absorpcję fluoru – sole glinu można zastosować w terapii ostrego zatrucia fluorem.
Kompleksy Al-F – wpływ na szkliwo i kości
Kompleksy Al-F tworzą się in vivo i in vitro. Glin, po tlenie i krzemie, jest trzecim najpowszechniejszym pierwiastkiem skorupy ziemskiej. Znajduje się w żywności i wodzie pitnej. Już przy stężeniach jonów Al3+ o wartościach mikromolowych mogą tworzyć się biologicznie efektywne kompleksy z jonem fluorkowym. Fluorek natomiast znajduje szerokie zastosowanie w ochronie przed próchnicą, zawierają go pasty do zębów oraz woda pitna. Dlatego powstawanie fluorku glinu powinno zostać gruntownie przebadane – to proces, który może wywierać istotny wpływ (fizjologiczny lub patologiczny) na biologię kości, fluorozę, choroby narządu żucia i in.
Fluorki są ściśle powiązane z fizjologią tkanek mineralizujących, szczególnie kości i szkliwa. W płytce nazębnej i w kieszeniach peridontalnych istnieją kwaśne warunki dla tworzenia kompleksów Al-F. Poza tym kompleksy te mogą atakować przyżyciowo bakterie jamy ustnej, przede wszystkim bakterie kwasogenne (i inne), przez hamowanie ATP-azy przenoszącej jony H+. Może to wywierać istotny wpływ na rozwój próchnicy i chorób przyzębia.
Udało się dowieść, że ATP-azę przenoszącą jony H+, izolowaną z błon bakterii jamy ustnej, może hamować fluorek. Ustalono ponadto, że hamowanie tego enzymu zależy wprost od obecności jonów Al3+. Mechanizm potwierdzono u człowieka na szczepach bakteryjnych jamy ustnej: ATP-aza przenosząca jony H+ może być chroniona przed hamowaniem przez fluorek w obecności chelatora jonów Al3+ – deferoksaminy. Wskazuje to, że fluorek może hamować ATP-azę zależną od H+ przez tworzenie kompleksu Al-F.
wiesz, że...
dentysta.eu
- Ostatni dzwonek, aby tanio wymienić plomby amalgamatowe na lepsze i zdrowsze
- Co pacjenci sądzą o dentystach i jak (nie)wiele na ten temat wiedzą stomatolodzy
- Zapowiedź wyników badania – czego oczekują pacjenci i co dentyści wiedzą o pacjentach
- Pacjenci – widma prześwietleni: wyniki ankiety o umawianiu wizyt
- Wyniki ankiety „Uśmiech a status społeczny”
forum
u nas!
 Wysoka odwiedzalność serwisu sprawia że bez problemu dotrzesz do swoich nowych klientów!
Wysoka odwiedzalność serwisu sprawia że bez problemu dotrzesz do swoich nowych klientów!
 Wystarczy że dodasz swój gabinet w ogłoszeniach portalu - szybko i zupełnie za darmo!
Wystarczy że dodasz swój gabinet w ogłoszeniach portalu - szybko i zupełnie za darmo!
 Dzięki promowaniu zyskają również Twoi klienci którzy łatwo Cię odnajdą!
Dzięki promowaniu zyskają również Twoi klienci którzy łatwo Cię odnajdą!
 Nadal się wahasz? Kliknij:
Dowiedz się więcej
Rozwiń
Nadal się wahasz? Kliknij:
Dowiedz się więcej
Rozwiń