Wyniki dla: układ odpornościowy
Zęby dotknięte próchnicą, zapaleniem miazgi lub z wytworzonym ropniem w pobliżu wierzchołka nie są błahym problemem. Zepsute zęby istotnie wpływają na stan naszego zdrowia fizycznego i psychicznego. Nikogo nie trzeba przekonywać, że zniszczone zęby nie dodają uroku, nie każdy jednak wie, że ząb dotknięty próchnicą lub objęty ropniem stanowi wrota infekcji dla wielu chorobotwórczych drobnoustrojów. Zakażenie może rozpoczynać się w miazdze zęba i rozprzestrzeniać się poprzez kanały zęba obecne w jego korzeniach do tkanek okołowierzchołkowych, skąd może dostawać się także do kości.
Zepsute zęby – ryzyko dla całego organizmu
Po dostaniu się do kości, o ile schorzenie nie jest leczone zaczyna się proces ropotwórczy, ropa zbiera się w wyniku odpowiedzi odpornościowej organizmu na inwazję mikroorganizmów, głównie bakterii. Zebrana ropa może pozostawać w kościach lub szukać ujścia przez tkanki miękkie – poprzez utworzenie przetoki, czyli rozerwania warstw mięśni, błon śluzowych i/lub skóry. Proces zapalny objawia się zwykle bólem, gorączką, dreszczami i pogorszeniem samopoczucia. Na zasięg zakażenia mają wpływ głównie rodzaj drobnoustroju (niektóre mikroorganizmy pozostają przez dłuższy czas w jednym miejscu, inne wędrują do coraz to nowych obszarów ciała) oraz poziom odporności – u osób odpornych infekcje rozprzestrzeniają się zwykle wolniej, niż u pacjentów z licznymi schorzeniami lub osób po przeszczepach poddanych immunosupresji.
Drogi szerzenia się zakażeń można podzielić na bezpośrednie i pośrednie. Infekcje szerzące się bezpośrednio obejmują przylegające do miejsca przebiegu zapalnego tkanki miękkie. W wyniku rozprzestrzeniania takiego zakażenia mogą się tworzyć ropnie – są to małe jamki ograniczone wałami tkankowymi, które zawierają martwe komórki, bakterie i leukocyty – białe ciałka krwi, które zwalczają drobnoustroje, są one otoczone dużą ilością ropy. Ropnie pochodzenia odzębowego można podzielić na ropnie okołowierzchołkowe, podokostnowe oraz podśluzówkowe.
Ropnie okołowierzchołkowe tworzą się najczęściej w wyniku głębokiej próchnicy i obumarcia miazgi zęba z wytworzeniem ropy, która wędruje kanałami w korzeniu zęba i przedostaje się przez wierzchołek korzenia – jeśli proces jest przewlekły, tzn. trwa długo w czasie, to stan zapalny dociera do kości i w jego wyniku zostaje ona rozpuszczona i powstaje pusta przestrzeń zwana torbielą lub cystą.
Ropnie podokostnowe, które są kolejnym po ropniach okołowierzchołkowych stadium zapalenia, gdy wydzielina ropna migruje przez kość docierając do okostnej i odwarstwiając ją, co jest bardzo bolesne. Ropnie podokostnowe są bardzo często zlokalizowane na podniebieniu, nie przechodzą wówczas w ropnie podśluzówkowe, natomiast są najbardziej bolesnymi ropniami ze wszystkich – ból często promieniuje na połowę twarzy, lub całą twarz, opisywany jest jako pulsujący i ciągły, może nasilać się w nocy.
Ropnie podśluzówkowe, których wydzielina wędruje przez okostną szczęki lub żuchwy i przebija błonę śluzową jamy ustnej lub skórę – proces ten zachodzi zawsze po najmniejszej linii oporu. W momencie perforacji błony śluzowej i wydostawania się ropy na zewnątrz następuje zmniejszenie się bólu – ma to związek ze zmniejszeniem się ciśnienia płynu wewnątrz ropnia. Procesowi temu towarzyszy gorączka, obrzęki policzków, jamy ustnej, warg i okolicy podoczodołowe. W zależności od zęba, który stał się przyczyną zakażenia otworzenie się ropnia następuje w innym miejscu, dla zębów szczęki jest to często przedsionek jamy ustnej (zakażenia z zębów przedtrzonowych i trzonowych), czyli przestrzeń między wargami a łukami i wyrostkami zębowymi, dół nadkłowy (występuje na wysokości kła – zakażenie pochodzi zwykle od zębów przednich, rzadziej os przedtrzonowców), zatoka szczękowa – znajduje się we wnętrzu kości szczękowej, jama nosowa, możliwe jest także przebicie się ropnia przez policzek (ropnie przy zębach trzonowych) i wylewanie się jego treści na skórę oraz utworzenie ropnia na podniebieniu (infekcja najczęściej od siekaczy bocznych lub pierwszych przedtrzonowców). Jeśli chodzi o perforację ropnia do zatoki szczękowej, to głównie ma to miejsce w przypadku wystąpienia infekcji 2. przedtrzonowca i 1. trzonowca szczęki, gdyż ich korzenie znajdują się najbliżej niej, a zdarza się nawet, że położone są w jej świetle. Ropnie pochodzące od zębów żuchwy otwierają się do przedsionka jamy ustnej, perforują jej dno, czyli okolicę pod językiem, oraz mogą drążyć przez policzek (głównie ropnie od korzeni zębów trzonowych) i brodę i przebijając skórę otwierać się na zewnątrz. Należy pamiętać, że jeżeli ból zęba z próchnicą był ciągły i trwał dość długo, a potem nagle się zakończył, to nie świadczy to o jego samowyleczeniu, a jest raczej sygnałem obumarcia miazgi, która zawiera nerwy informujące o jego złym stanie, wraz ze śmiercią komórek nerwowych dane o stanie zapalnym przestają do nas docierać. Po tym okresie zwykle pojawia się ból na nagryzanie – jest to związane z pojawieniem się ropnia okołowierzchołkowego i zapaleniem ozębnej. Ból ten utrzymuje się jakiś czas a następnie stopniowo ustępuje – dzieje się tak, ponieważ ropa zbierana w okolicy okołowierzchołkowej korzenia zęba znajduje ujście do kości, skąd dalej się rozprzestrzenia, aż wytworzy przetokę i wyleje wydzielinę ropną – do wnętrza jamy ustnej przez błonę śluzową lub na zewnątrz przez otwór w skórze. Dlatego nie należy czekać, aż przestanie boleć – lepiej udać się do stomatologa, który nas przebada i ustali przyczynę bólu i rozpocznie leczenie, oczekiwanie, że ból i zapalenie minie nie jest wskazane, gdyż może doprowadzić do poważniejszych konsekwencji, niż utrata zębów.
Infekcja może też rozprzestrzeniać się poprzez błonę śluzową jamy ustnej i skórę i tworzyć przestrzenie patologiczne z nią połączone, lub też rozsiewać się w tkankach miękkich wywołując cellulitis. Cellulitis jest to rozproszone zapalenie tkanek miękkich podskórnych lub leżących pod błonami śluzowymi, nie jest ono ograniczone i w przeciwieństwie do ropni rozprzestrzenia się poprzez naturalne przestrzenie oraz wzdłuż powięzi mięśniowych, czyli błon, które pokrywają mięśnie. Nie należy mylić tego rodzaju zapalenia z pomarańczową skórką, na którą często skarżą się kobiety, ponieważ oba te stany, oprócz nieciekawego wyglądu, nie mają ze sobą żadnego związku. Ten rodzaj zakażenia stosunkowo szybko przenosi się dalej, obejmując coraz większą ilość tkanek. W niektórych przypadkach stan ten może wywołać ciężką niewydolność oddechową, dzieje się tak, gdy infekcja przenosi się w okolice szyi i wywołuje obrzęk, który zmniejsza światło dróg oddechowych. Stan zapalny może się także przenosić z tkanek miękkich do wnętrza kości wyrostków zębodołowych i wywoływać tam zapalenie szpiku kostnego. Ogniska zapalne w jamie ustnej, takie jak zepsute zęby, mogą także doprowadzać do zapaleń zatok nosowych i czołowych. Więcej
Nawet drobne zabiegi stomatologiczne mogą powodować, że do naszego krwioobiegu przedostaną się bakterie. Podczas, gdy jeden organizm z chwilowego zakażenia krwi wyjdzie bez szwanku, w drugim bakterie mogą spowodować sepsę, a nawet doprowadzić do śmierci. Skąd wiedzieć jak na bakteriemię może zareagować nasz organizm?
Bakteriemia zębopochodna – co to takiego?
Bakteriemia zębopochodna to stan zakażenia krwi bakteriami bytującymi w jamie ustnej lub przeniesionymi na narzędziach dentystycznych. Do zakażenia może dojść, gdy przerwana zostanie ciągłość naczyń krwionośnych w błonach śluzowych lub dziąsłach. To z kolei może nastąpić nie tylko na skutek zabiegów dentystycznych takich jak leczenie kanałowe, płukanie kieszeni przyzębnych, nacięcie ropnia albo ekstrakcja zęba, ale nawet w wyniku zwykłej, codziennej higieny jamy ustnej, obejmującej szczotkowanie zębów czy używanie nici dentystycznej.
Bakteriemia zębopochodna, która powstaje we wcześniej wspomnianych przypadkach, przyjmuje postać przejściową. Oznacza to, że drobnoustroje obecne są we krwi jedynie przez 5-15 minut i nie dochodzi do późniejszych nawrotów infekcji. U większości osób bakteriemia przejściowa nie powoduje żadnych objawów ani powikłań zdrowotnych, ale dla niektórych może stanowić nawet śmiertelne zagrożenie. Więcej
Stany zapalne w przyzębiu wiążą się ze zaktywowaniem komórek układu odpornościowego, w tym regulatorowych limfocytów T. Właśnie dowiedzieliśmy się, że zachowanie tych komórek stanowi klucz do zrozumienia, dlaczego podczas zapalenia przyzębia dochodzi do postępu tej choroby pomimo wzrostu liczby limfocytów T w okolicy objętej stanem zapalnym.
Regulatorowe limfocyty T zaangażowane są w ochronę tkanek przyzębia przed niszczeniem w procesie zapalnym. Mogą jednak zacząć zachowywać się w zupełnie nieoczekiwany dla nich sposób – zamiast chronić kości przyzębia przed zniszczeniem, zaczynają aktywnie działać na rzecz promowania toczącego się w przyzębiu stanu zapalnego. Komórki te tracą swoje zdolności supresyjne i w rezultacie – zamiast efektywnie pomagać – skutecznie szkodzą, doprowadzając do utraty masy kostnej w obszarze przyzębia objętym procesem zapalnym.
Odkrycia tego dokonali uczeni z Instytutu Forsytha w USA i Uniwersytetu w Chile. Jest ono niczym kolejny puzzel, który dołożony zostaje do niezwykle skomplikowanej układanki odnoszącej się do wciąż niezrozumiałej do końca roli układu immunologicznego w procesie utraty masy kostnej w zapaleniu przyzębia, ale również i w innych schorzeniach, jak na przykład w osteoporozie czy reumatoidalnym zapaleniu stawów. Więcej
Próchnica zębów to współcześnie najbardziej rozpowszechniona zakaźna choroba cywilizacyjna. Jest schorzeniem wieloprzyczynowym, które spowodowane jest wzajemnym oddziaływaniem czynników z wielu obszarów: środowiska, genów, zachowań. Owo współoddziaływanie dotyczy czterech podstawowych elementów: gospodarza, substratu, bakterii, czasu. I każdy z wymienionych elementów ma swój udział w budowaniu odporności na próchnicę – choć u konkretnej osoby każdy z tych czynników będzie się cechował różną siłą wpływu.
Wieloczynnikowa odporność na próchnicę
Odporność na próchnicę warunkowana jest przez następujące elementy:
- Osobnicze właściwości zębów i szkliwa – wynikają z predyspozycji genetycznych konkretnej osoby i jej wieku[1]. Pewne choroby genetyczne mają lub mogą mieć wpływ na odporność zębów na próchnicę, ponieważ skorelowane są z występowaniem np. niedorozwoju szkliwa czy wad zgryzu. Udowodniono też, że na dobrą odporność szkliwa wpływa odpowiednie ułożenie hydroksyapatytów w krystalicznej siatce minerałów tworzących tę tkankę[2]. Uformowanie powierzchni żujących zębów także może silnie kształtować odporność na próchnicę – powierzchnię, którą charakteryzują bruzdy szerokie i płytkie, łatwiej i skuteczniej oczyszcza się z zalegającego na niej osadu niż tę z bruzdami głębokimi, z których trudniej usunąć nalot nazębny.
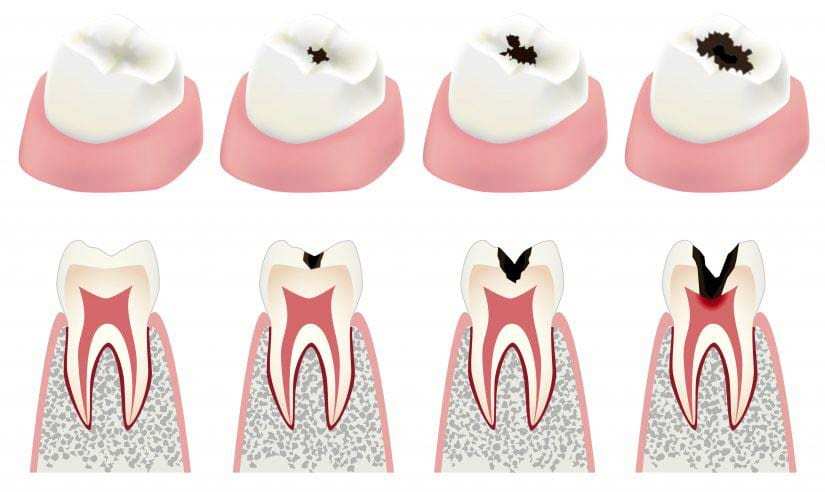 etapy próchnicy – wcześnie wykryta może uniknąć leczenia kanałowego
etapy próchnicy – wcześnie wykryta może uniknąć leczenia kanałowego
Paradontoza i inne postaci przewlekłego zapalenia przyzębia przez długie lata uznawano głównie za choroby związane z wiekiem. Kolejne badania naukowe potwierdzały jednak, że za destrukcję tkanek utrzymujących zęby w karnym łuku i w kości szczęk odpowiedzialne są bardziej drobnoustroje niż liczba przeżytych lat. Jednym z mikroorganizmów izolowanych z patologicznych kieszonek dziąsłowych była bakteria Porphyromonas gingivalis. Ta niewielka Gram ujemna pałeczka, którą po raz pierwszy opisano w 1921 roku, wygląda niepozornie. Rosnąc na pożywkach w warunkach laboratoryjnych, może tworzyć zielonkawe, interesujące pod względem kształtu kolonie. Na początku XXI wieku uznawana była już za jeden z gatunków silnie powiązanych z chorobami dziąseł i przyzębia.1 Obecnie wiadomo, że to wróg numer 1 zdrowia tkanek przyzębia. Jej siła działania ukrywa się między innymi w wytwarzanych przez nią gingipainach. To enzymy, dzięki którym bakteria nie tylko pozyskuje dostęp do potrzebnych jej składników odżywczych. Ułatwiają one również przyczepianie się P. gingivalis do tkanek i – co najistotniejsze – potrafią modulować działanie układu immunologicznego gospodarza, kierując jego ataki na swoje własne tkanki a nie na niszczące przyzębie patogeny. Warto podkreślić, że im bardziej zaawansowana destrukcja tkanek przyzębia, tym większy udział populacji P. gingivalis w całej puli mikroorganizmów patogennych izolowanych z chorych obszarów.
W badania nad P. gingivalis już od wielu lat mocno angażuje się prof. Jan Potempa, biochemik i mikrobiolog. Za swoją pracę w tym obszarze odebrał w 2011 r. nagrodę Fundacji na rzecz Nauki Polskiej zwaną polskim Noblem.
Porphyromonas gingivalis – niszcząca moc o wymiarach mikro
Bakteria P. gingivalis uznawana jest za najbardziej wirulentny i patogenny drobnoustrój w swojej grupie, a coraz więcej wyników badań potwierdza jej negatywny wpływ nie tylko na zdrowie tkanek przyzębia, ale również na zdrowie ogólne. Zjadliwość i skuteczność tego gatunku bakterii zapewniają:
- Gingipainy – gatunek wytwarza dwie różne klasy tych enzymów. Ich rolą jest:
- Wspomaganie pozyskiwania składników pokarmowych. Z enzymatycznego rozkładu dużych peptydów znajdujących się w osoczu krwi człowieka komórki gingivalis uzyskują pokaźne ilości azotu i węgla, a z rozkładu transferyny – wystarczającą ilość żelaza, które jest niezbędne do zapewnienia aktywności określonych szlaków metabolicznych w komórkach tych patogenów.2
- Wspomaganie inwazji i kolonizacji ciała gospodarza, czyli związanych z tym sił kohezji i adhezji. Dzięki tym siłom komórki bakteryjne mogą przyczepiać się do tkanek, a jednocześnie ściśle przylegać do siebie, co korzystnie wpływa na tworzenie, dojrzewanie i utrzymywanie struktury biofilmu.
- Osłabianie i modulowanie odpowiedzi immunologicznej gospodarza. Gingipainy działają tu na różne sposoby, m.in. modulują aktywność przeciwciał klasy IgG oraz cytokin prozapalnych, hamują dojrzewanie limfocytów T, a także zakłócają komunikację między komórkami i macierzą oraz hamują namnażanie się komórek odpornościowych.
- Niszczenie metaloprotein, kolagenu i fibronektyn, przez co komunikacja na linii komórki – macierz pozakomórkowa jest utrudniona lub blokowana.3 Tym samym gingipainy utrudniają wytwarzanie i transport czynników uczestniczących w zwalczaniu stanów zapalnych i biorących udział w regeneracji tkanek. Skutkiem tego jest postępująca degradacja tkanek przyzębia.
- Polisacharydowa kapsuła – warunkuje większą zjadliwość bakterii oraz zapobiega wchłonięciu patogenów przez fagocytujące komórki układu immunologicznego.
- Fimbrie – te niewielkie wypustki mają kluczowe znaczenie dla adhezji i kohezji komórek bakteryjnych oraz dla zapewnienia właściwej struktury biofilmu. Są też niezbędne do kolonizacji środowiska. Fimbrie długie odpowiadają za przyczepienie się bakterii do podłoża i za organizację biofilmu w pierwszych etapach jego powstawania. Z kolei fimbrie krótkie odgrywają istotną rolę w agregowaniu komórek i tworzeniu mikrokolonii oraz wielogatunkowych zespołów złożonych z różnych mikroorganizmów zasiedlających jamę ustną. Fimbrie wchodzą także w interakcje z białkami osocza oraz z receptorami chemokin, przez co – równolegle do gingipain – modulują odpowiedź immunologiczną gospodarza.
- Zwiększanie wirulencji innych patogennych gatunków bakterii zamieszkujących jamę ustną – gingivalis potrafią tworzyć zespoły z innymi bakteryjnymi patogenami żyjącymi w jamie ustnej i modyfikować ich funkcjonowanie tak, że te skuteczniej radzą sobie z niszczeniem tkanek przyzębia.
Skutki działania P. gingivalis
Gatunek P. gingivalis żyje głównie w nazębnej płytce poddziąsłowej (najczęściej wykrywa się go u osób z ciężkimi postaciami przewlekłych zapaleń przyzębia), ale także w ślinie, na śluzówce jamy ustnej, języku i migdałkach. Migdałki uznaje się za rezerwuar tego drobnoustroju. Poza jamą ustną bakteria ta znajdowana jest sporadycznie, ale może ona infekować narządy leżące daleko od tego obszaru ciała. Do takiej sytuacji dojdzie, kiedy P. gingivalis przedostanie się do krwiobiegu i wraz z krwią dotrze np. do nerek. Może tam wytworzyć wtórne ogniska zakażenia. P. gingivalis może zatem działać lokalnie – niszcząc tkanki przyzębia, ale też ogólnoustrojowo – co potwierdzają liczne doniesienia naukowe.
Szkodliwa skuteczność P. gingivalis wynika z dużej zdolności do przyczepiania się bakterii do nabłonka jamy ustnej oraz z aktywowania komórek – już nie tylko nabłonka, ale również śródbłonka, czyli warstwy wyściełającej naczynia.4 To dlatego bakteria jest tak skuteczna nie tylko w niszczeniu przyzębia, ale również w degradacji tkanki naczyniowej.
Najnowsze odkrycia naukowe potwierdzają związki P. gingivalis z następującymi zaburzeniami zdrowia:
- Choroby układu sercowo-naczyniowego – m.in. miażdżyca i choroba wieńcowa.
- Choroby układu oddechowego – m.in. zapalenie płuc.
- Choroby układu nerwowego – m.in. stwardnienie rozsiane.
- Zaburzenia przebiegu ciąży – m.in. przedwczesny poród, niska masa ciała noworodków.
- Choroby układu ruchu i autoimmunologiczne – m.in. reumatoidalne zapalenie stawów (RZS).
- Schorzenia onkologiczne – m.in. nowotwór trzustki.
Przychodzi pacjent do stomatologa, skarżąc się na dokuczliwe stany zapalne w jamie ustnej czy zesztywnienie stawów skroniowo-żuchwowych i zostaje zaskoczony sugestią, że cierpi na… schorzenie jelit, konkretnie chorobę Leśniowskiego-Crohna. Dentysta może stać się pierwszym lekarzem, który zdiagnozuje to schorzenie, ponieważ to nieswoiste zapalenie jelit, dotykające najczęściej ludzi młodych między 20. a 30. rokiem życia, może dawać objawy praktycznie w każdym odcinku przewodu pokarmowego: od jamy ustnej po odbyt. Ponadto symptomy w jamie ustnej mogą pojawić się nawet na kilka miesięcy przed wystąpieniem jelitowych objawów choroby – co notuje się u 8-29 proc. pacjentów dotkniętych chorobą Leśniowskiego-Crohna.1
Przyczyny choroby Leśniowskiego-Crohna
Choroba Leśniowskiego-Crohna wraz z wrzodziejącym zapaleniem jelita jest jednym z najczęściej występujących schorzeń jelit. Przyczyny tego schorzenia nie zostały jeszcze jednoznacznie określone, ale wskazuje się na:
- czynniki genetyczne – to główny podejrzany, ponieważ notuje się rodzinny charakter choroby, a na chromosomie 16 znaleziono geny, które warunkują podatność na wystąpienie schorzenia;
- zaburzenia w układzie odpornościowym związane głównie z jelitami – dysfunkcja ma charakter choroby immunologicznej, ponieważ powoduje wzrost aktywności limfocytów T-pomocniczych, czyli tych, które wspomagają odpowiedź odpornościową organizmu;
- zakażenie drobnoustrojami, np. Mycobacteruim paratuberculosis – według jednej z nowych teorii mikroorganizmy wykorzystują dwa fakty, które sprzyjają zakażeniu i rozwojowi choroby Leśniowskiego-Crohna: przejściowe osłabienie śluzówki jamy ustnej oraz zakłócenie zdolności do usunięcia patogennych bakterii ze ścianki jelit;
- niedobory pokarmowe będące wynikiem istnienia choroby.
Kobiety i mężczyźni są w porównywalnym stopniu podatni na rozwój schorzenia, ale amatorzy nikotynowego dymka są dwukrotnie częściej narażeni na pojawienie się choroby Leśniowskiego-Crohna niż osoby niepalące.2 To istotna uwaga, ponieważ palenie tytoniu jest czynnikiem o bardzo silnym negatywnym wpływie własnym na zdrowie jamy ustnej: sprzyja powstawaniu nowotworów, wywołuje przebarwienia zębów oraz jest powodem nieświeżego oddechu.
Rozwojowi schorzenia sprzyjają także3:
- pochodzenie żydowskie lub europejskie (szczególnie mieszkańcy Skandynawii);
- życie na terenach miejskich;
- dieta uboga w warzywa i owoce, a bogata w cukier i tłuszcze nasycone;
- nadwaga lub otyłość;
- niska ekspozycja na światło słoneczne.
O związkach chorób jamy ustnej z miażdżycą i jej konsekwencjami: zawałem lub udarem zrobiło się głośno kilka lat temu, kiedy coraz więcej badań wskazywało na fakt, że bakterie z chorych zębów i przyzębia wybitnie przyczyniają się do powstania blaszki miażdżycowej i zwężania światła naczyń tętniczych. Utrudniają w ten sposób lub uniemożliwiają krwi swobodny przepływ i sprzyjają powstawaniu skrzepów. Konsekwencją ostateczną ograniczenia przepływu krwi lub zablokowania przez skrzep naczynia krwionośnego jest zgon. Brzmi to poważnie, ale też bakterie, które wywołują próchnicę lub zapalenia przyzębia, kiedy przedostaną się do krwiobiegu, potrafią być bardzo niebezpieczne dla zdrowia ogólnego.
Przyjrzyjmy się bliżej procesowi powstawania blaszki miażdżycowej i mechanizmom prowadzącym do zamknięcia światła naczynia krwionośnego – zakładamy, że zrozumienie tych zależności u niejednej osoby zmieni zapatrywanie na tak prozaiczną czynność, jaką jest codzienne szczotkowanie zębów, i na konieczność okresowego kontrolowania zdrowia jamy ustnej.
- Zakażenie bakteriami
Powstawanie zmian miażdżycowych jest ściśle związane z infekcją i związanym z tym pobudzeniem układu odpornościowego oraz powstaniem procesu zapalnego. Bakterie, które mogą przedostać się do krwiobiegu z chorych zębów lub przyzębia, należą do szczepów, które skutecznie aktywują procesy immunologiczno-zapalne. To beztlenowe paciorkowce, gronkowce oraz wróg numer 1 zdrowia tkanek przyzębia – Porphyromonas gingivalis. Groźny jest też szczep Fusarium. Więcej
W Polsce coraz częściej obserwuje się niepokojący wzrost występowania zmian próchnicowych w zębach mlecznych u coraz młodszych dzieci. Zjawisko wczesnego zniszczenia koron zębów u najmłodszych w naszym kraju ma tak poważną skalę, że coraz częściej wdrażane są samorządowe programy prewencyjne już w przedszkolach. Choroba próchnicowa u dzieci jest schorzeniem wieloczynnikowym, na podatność na próchnicę wpływ mają zarówno zjawiska, jakie miały miejsce w czasie życia płodowego, jak i te, które nastąpiły po porodzie. Prowadzone od lat badania czynników sprawczych i przebiegu choroby próchnicowej u dzieci wykazały, że duży wpływ na jej rozwój i przebieg mają nie tylko dieta i przyzwyczajenia higieniczne, ale i podłoże genetyczne.
Czynniki wpływające na podatność na występowanie zmian próchnicowych u dzieci można podzielić na szereg grup. Do ważnych czynników należą nawyki higieniczne w rodzinie, sposób urodzenia dziecka, współistnienie chorób układowych i zespołów genetycznych, dieta oraz kontrola stomatologiczna. W polskim społeczeństwie wciąż jeszcze dość często pokutuje stereotyp, że pielęgnacja zębów mlecznych nie jest ważna, ponieważ wcześniej czy później zostaną one zastąpione przez zęby stałe. Z tego powodu wiele dzieci zgłasza się do stomatologa bardzo późno, co skutkuje w wielu przypadkach nie tylko zniszczeniem koron zębów mlecznych, powikłaniami w postaci ropni oraz zaburzeń zgryzu i proporcji twarzy, ale również niesie ze sobą zwiększone ryzyko rozwoju próchnicy w niedojrzałych zębach stałych.
Proces wykształcania zawiązków zębowych rozpoczyna się bardzo wcześnie, bo już w 4. tygodniu ciąży, dlatego jej przebieg jest istotnym czynnikiem prognostycznym w kierunku podatności na chorobę próchnicową. Do najistotniejszych czynników branych pod uwagę w analizie ryzyka zapadalności na próchnicę należy przyjmowanie leków w czasie ciąży, przebyte przez matkę choroby jak i jej dietę. Wiele z zaburzeń mineralizacji tkanek twardych zęba jest postrzeganych jako wynik niedoborów pokarmowych w czasie ciąży. Dzieci z ciąży mnogiej są również podatniejsze na objęcie zębów próchnicą niż w przypadku ciąży pojedynczej.
Według przeprowadzonych badań duży wpływ na podatność na próchnicę ma poród. U dzieci, które przyszły na świat siłami natury obserwuje się o wiele późniejszą kolonizację jamy ustnej przez bakterie z gatunku Streptococcus mutans, które są uważane za głównego sprawcę procesów próchnicowych. U dzieci, które urodziły się poprzez cesarskie cięcie kolonizacja jamy ustnej przez ten rodzaj bakterii następuje statystycznie o 11 miesięcy wcześniej niż w przypadku dzieci urodzonych naturalnie. Badacze wiążą ten fakt z nabywaniem większej odporności na różne rodzaje bakterii występujące w drogach rodnych matki podczas porodu. Uważa się, że szczepy bakteryjne, które wcześniej zasiedlą jamę ustną walczą z kolejnymi napotykanymi szczepami o przestrzeń życiowa, przez co na zasadzie konkurencji ustalana jest ich dominacja. U dzieci, które poprzez cesarskie cięcie zostały pozbawione styczności z takimi szczepami bakterii, w związku z aseptycznymi warunkami przeprowadzenia zabiegu konkurencja pomiędzy szczepami bakterii jest mniejsza, przez co bakterie z gatunku Streptococcus mutans mają łatwiejszą drogę do dominacji w środowisku jamy ustnej, co odbija się znacząco na podatności na próchnicę w ciągu dalszego rozwoju dziecka.
Dla podatności na próchnicę istotne znaczenie jest przypisywane także masie urodzeniowej dziecka oraz terminowi porodu. Wiele badań wskazuje na to, że niska masa przy urodzeniu zwiększa w dużym stopniu ryzyko wystąpienia choroby próchnicowej u dziecka. Także przedwczesny poród jest negatywnym czynnikiem prognostycznym, u dzieci urodzonych przed 37. tygodniem ciąży obserwuje się o wiele większą podatność na chorobę próchnicową niż u dzieci, które przyszły na świat po 37. tygodniu ciąży.
U dzieci, u których występują zaburzenia mineralizacji lub wykształcania tkanek o podłożu genetycznym ryzyko objęcia zębów próchnicą jest istotnie większe. Również niedorozwój psychofizyczny jest czynnikiem, który znacznie wpływa na stan higieny jamy ustnej, ponieważ niezborność ruchów i upośledzenie umysłowe znacznie utrudniają przeprowadzenie zabiegów higienicznych. Więcej
wiesz, że...
dentysta.eu
- Ostatni dzwonek, aby tanio wymienić plomby amalgamatowe na lepsze i zdrowsze
- Co pacjenci sądzą o dentystach i jak (nie)wiele na ten temat wiedzą stomatolodzy
- Zapowiedź wyników badania – czego oczekują pacjenci i co dentyści wiedzą o pacjentach
- Pacjenci – widma prześwietleni: wyniki ankiety o umawianiu wizyt
- Wyniki ankiety „Uśmiech a status społeczny”
forum
u nas!
 Wysoka odwiedzalność serwisu sprawia że bez problemu dotrzesz do swoich nowych klientów!
Wysoka odwiedzalność serwisu sprawia że bez problemu dotrzesz do swoich nowych klientów!
 Wystarczy że dodasz swój gabinet w ogłoszeniach portalu - szybko i zupełnie za darmo!
Wystarczy że dodasz swój gabinet w ogłoszeniach portalu - szybko i zupełnie za darmo!
 Dzięki promowaniu zyskają również Twoi klienci którzy łatwo Cię odnajdą!
Dzięki promowaniu zyskają również Twoi klienci którzy łatwo Cię odnajdą!
 Nadal się wahasz? Kliknij:
Dowiedz się więcej
Rozwiń
Nadal się wahasz? Kliknij:
Dowiedz się więcej
Rozwiń

